金属3D打印技术钛合金多孔材料——医疗领域篇
3D打印多孔植入物用于骨缺损治疗是组织工程领域的一项新突破。利用3D打印技术,可对植入材料的孔隙尺寸、孔隙率、孔隙形状及表面形貌等物理参数进行精确的微孔设计,这种优势是传统骨植入支架难以比拟的,因此可以制作出生物相容性和机械性能更为理想的个性化植入物,充分满足患者需求。
为什么选钛合金(钛合金的发展历程)
钛及钛合金,是20世纪中期才逐渐开始发展起来的一种金属材料。其拥有密度低,比强度高,耐蚀性能好,生物相容性好等特点,被广泛应用于航空航天、石油化工和医疗健康领域。
第一阶段
对于钛在医疗植入上的应用,早在1940年,就有学者报道了钛植入物与小鼠股骨之间的惰性表现。1951年,又有学者进一步证实了纯钛相比其他传统植入物材料,拥有更好的的生物相容性能。但由于当时钛合金生产成本高昂,不锈钢在植入体市场已较成熟等原因,钛合金在医学领域的应用发展一直较为缓慢。
第二阶段
自20世纪60年代,纯钛开始作为人体植入物被应用于临床口腔研究。随着具有更加优异使用性能的Ti-6Al-4V合金的开发,钛合金开始被广泛应用于医用植入物市场。
面临的问题
虽然Ti-6Al-4V的弹性模量仅为114GPa左右,较不锈钢、钴铬合金等其他生物材料低,但仍比人体皮质骨(15~25GPa)和松质骨(0.05~3GPa)高出一个数量级。如此大的差异会导致所谓的“应力屏蔽”效应发生,长期将会导致植入体周围骨吸收,甚至导致植入体的滑落,降低骨植入的成功率。
“应力屏蔽”效应指生物植入体弹性模量(>100GPa)与受体骨弹性模量(<20GPa)的数值差异较大,导致植入体受力后变形程度与骨不一致,长期使用会引起植入体周围骨质疏松与骨消融,最终导致植入体滑落的现象。适当降低弹性模量的方法是近年来生物材料研究学者的工作重点之一。通常,降低弹性模量的方法包括采用弹性模量较低的合金或利用多孔设计降低其零件强度。
同时,其成分中所包含的Al、V等元素,均具有一定的生物毒性,长期在人体内使用会引起植入体周围组织病变,诱发脑病、贫血等症状,并不适合长期在人体内使用。
解决方案
生物毒性方面
近年来,针对生物用钛合金,研究学者围绕无毒、低弹性模量等特性,开发了诸如含有Ti-Nb-Ta-Zr的Gum合金、含有Ti-Nb-Zr-Mo-Sn的TLM合金以及含有Ti-Nb-Zr-Sn的Ti2448合金等等,这些合金均采用了生物相容性较好的Nb、Zr、Mo等元素。有实验结果表明,此类钛合金的骨促进性、致敏性等生物学表现均优于传统植入物所采用的Ti-6Al-4V与Ti-6Al-7Nb。
应力遮蔽方面
有研究数据表明,多孔材料的开发可有效地降低弹性模量,且为骨长入提供物理空间,增强骨固定。对于骨植入多孔材料,有学者报道,其孔隙率应控制在65%~80%之间。对于孔隙率过大的植入体材料,孔隙率会显著降低材料的抗压强度与疲劳性能,几乎无法满足材料的正常使用需求;而低于这一值的多孔材料,由于致密度较高,影响骨组织长入材料内部,降低植入体与材料的结合强度。
传统方法VS 3D打印的对比
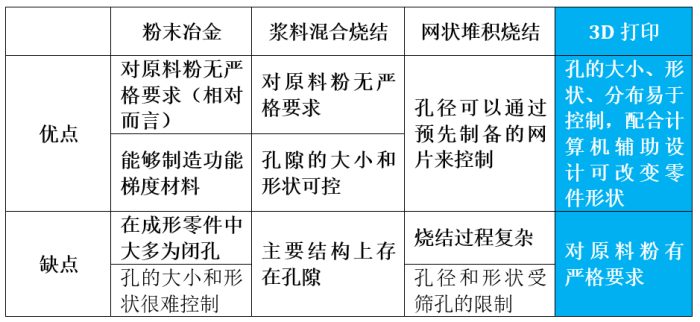
为达到上述材料孔隙率的设计需求,传统的多孔钛合金材料制备方法主要包括如:粉末冶金法,浆料法和纤维烧结法等。
但此类方法制作的多孔材料普遍孔径较小,孔隙分布不均匀,通孔率不高,或孔壁结构上存在大量微孔,限制了其在生物材料领域的进一步发展。近年来,随着“3D打印”技术的提出,因其加工的特点,用3D打印来制造多孔材料的优势越发明显。
下表对比了几种常见多孔材料制备方法的特点,图XX则展示了造孔剂烧结法与3D打印SLM工艺从原材料到成形产品的异同。
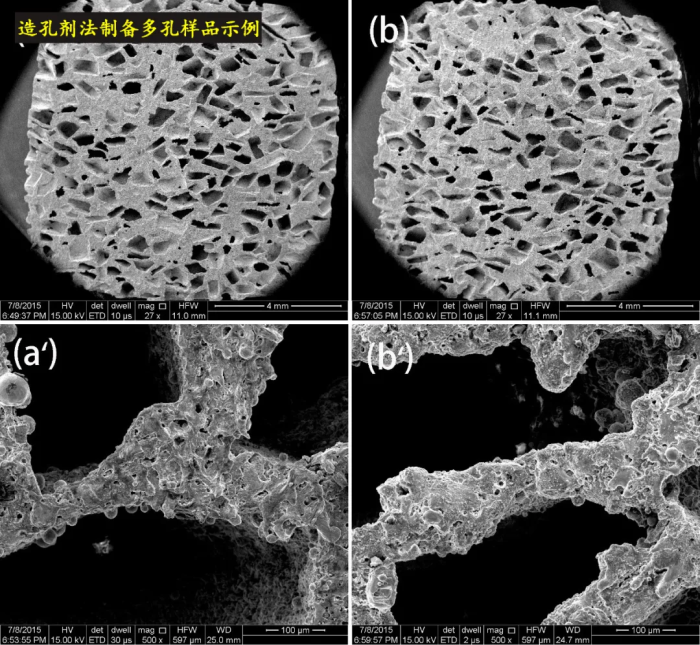
造孔剂法使用粉末 VS SLM工艺使用粉末


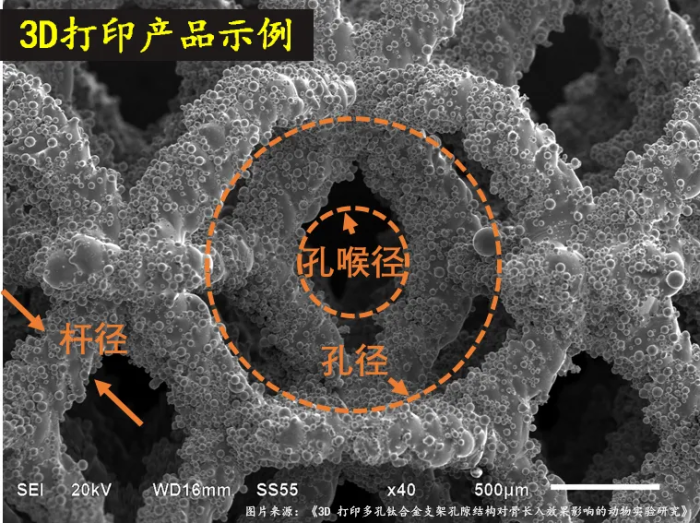
造孔剂法制备多孔样品 VS 3D打印产品
常见骨小梁胞元结构的三维模型示例

未来,随着多孔材料孔隙率和孔径大小、弹性模量、生物毒性等问题的解决,以及各学科包括材料学、干细胞技术等的整合与突破,3D打印钛合金替代物将会成为一种个性化、精准化的医疗技术,广泛应用于骨科临床,有效地解决骨修复的治疗难题。
镭明激光钛合金打印案例


参考文献:
《3D打印钛合金骨小梁多孔结构的拉伸性能》
《3D 打印多孔钛合金支架孔隙结构对骨长入效果影响的动物实验研究》
《3D 打印医用钛合金研究进展》
热点文章
-
“共启新篇章,携手迎未来” —魏因加特纳北京乔迁仪式暨2025新春茶话会圆满落幕
2025-01-15
-
破解产线测量痛点,雷尼绍五轴测量助推产业提质增效
2025-01-10
-
专注笃定二十载,闪耀无境新征途 | 先临三维20周年庆典暨新研发生产基地启用仪式圆满举行
2025-01-13
-
蔡司自动化解决方案:提升企业效率的智能化伙伴
2025-01-14
-
新春福利 | 三坐标探针系统以旧换新,助您生产力翻倍!
2025-01-14
-
蔡司智能服务看板助力稳定、高效使用三坐标
2025-01-14
-
首批!海克斯康获批国家工信部卓越级智能工厂
2025-01-13
-
国产刀具品牌崛起:这三家刀具新势力何以致胜?——机械工业科技创新领航奖调研行(苏浙篇)
机械工业科技创新领航奖调研团携同刀具行业专家、哈尔滨理工大学刘献礼教授一同走访了三家国产品牌的代表性刀具企业:沃尔德、松德刀具和国宏工具,与之进行了深度交流,实探其研发创新及工厂生产状况,着实让人看到了中国刀具企业奋起直追的精神和打造科技创新的硬实力所在。
作者:何发
-
无限微来 智领前行 微茗智能开放日暨乔迁庆典活动成功举办
-
无限微来 智领前行 | 微茗智能开放日暨乔迁庆典活动成功举办
-
传承创新基因 打造高质标杆——伊斯卡LOGIQUICK新品盛典在苏州成功举办
-
开放包容·互联互通 打造智能制造 示范生态圈
-
汇聚行业精英 共谋创新发展——无锡航空航天先进制造技术与工艺研讨会成功举办















评论
加载更多